膳食油脂是人體攝入的重要營養成分,主要由甘油三酯(triglycerides)、磷脂(phospholipids)、膽固醇(cholesterol)、脂溶性維生素等構成。作為人體不可缺少的一類營養素,其代謝和吸收在營養學領域中占據重要地位。它們在提供能量、構建細胞膜以及維持體內多種生理功能中扮演關鍵角色。然而,由于油脂不溶于水,其消化和吸收過程相對復雜,需要經歷乳化、酶解、轉運、細胞內代謝及轉運至體循環等多個生理步驟。以下將詳細解析膳食油脂在腸道中的消化吸收過程。
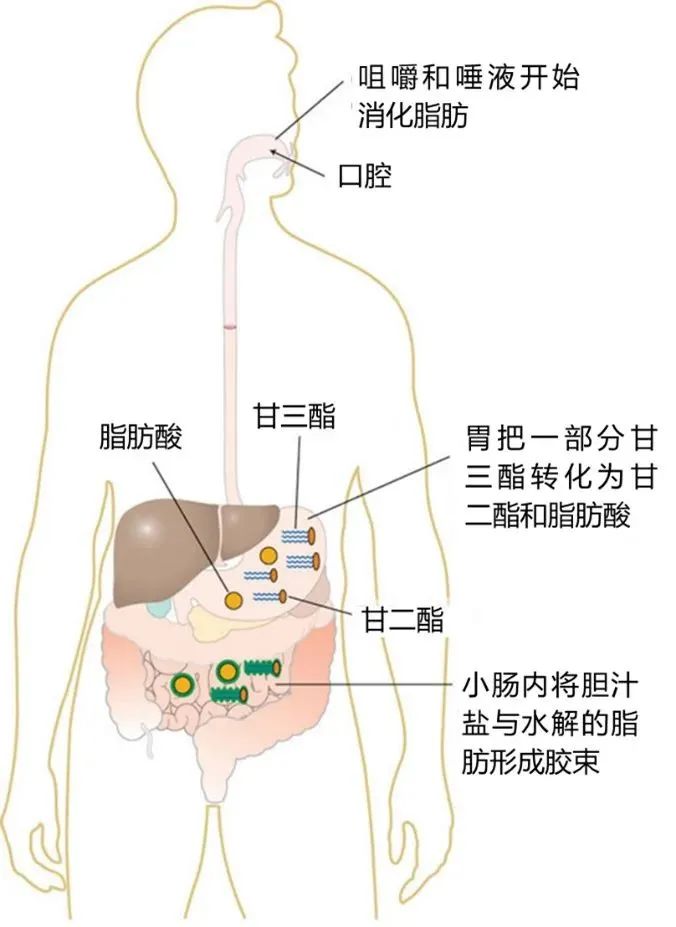
膳食油脂在腸道中消化吸收過程示意圖
1. 膳食油脂在胃腸道的消化
膳食油脂的消化分為口腔消化、胃消化和小腸消化過程,舌脂肪酶及胃脂肪酶可以水解短鏈甘油三脂,隨后進入小腸后,通過小腸蠕動,在膽汁中的膽汁酸鹽的作用下使油脂發生乳化作用。膽汁酸是兩性分子,一端親水、一端疏水,它們能夠將不溶于水的脂肪大顆粒分解為更小的脂肪滴,從而增加脂質與消化酶的接觸表面積,有利于脂類的消化與吸收。乳化完成后,胰脂肪酶(pancreatic lipase)與其他輔助因子如共脂肪酶相互作用,水解甘油三酯,將其分解為2-單酰甘油(2-monoglycerides)和游離脂肪酸(free fatty acids),這些脂質產物能夠被腸道上皮細胞吸收。此外,膽固醇酯和磷脂分別在膽固醇酯酶和磷脂酶A2的作用下被水解為游離膽固醇和溶血磷脂,從而準備進入吸收階段。
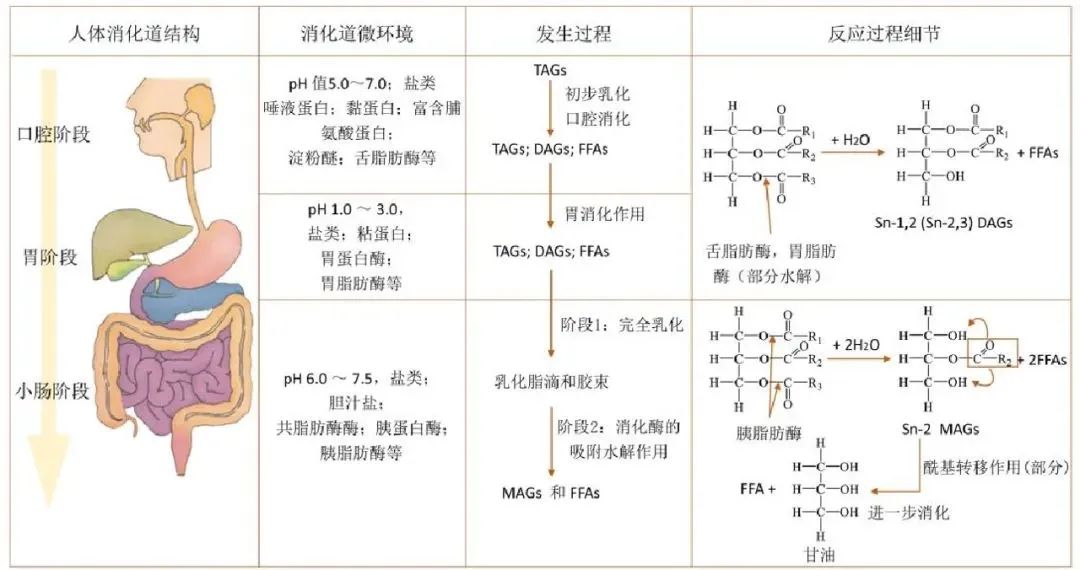
人體消化結構與膳食油脂在胃腸道中的消化過程
2. 膳食油脂在小腸中的吸收
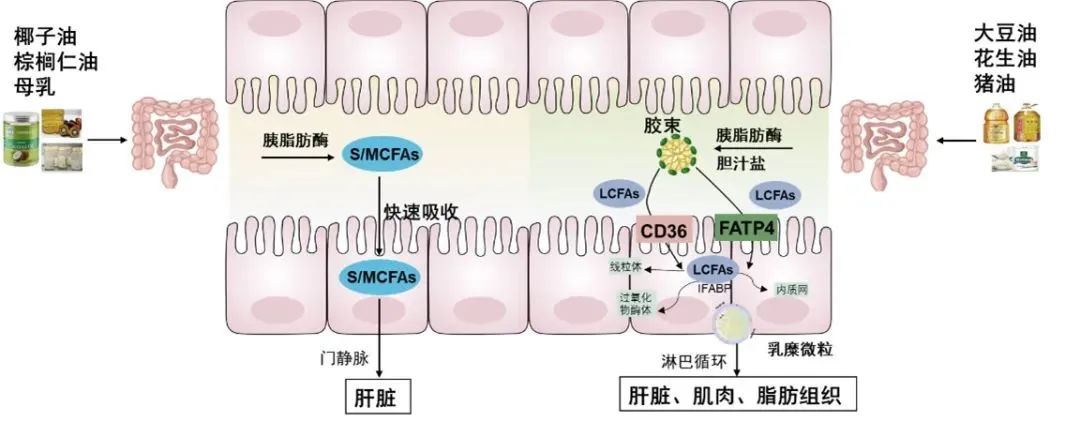
乳化后的脂質產物與膽汁酸形成混合膠束(mixed micelles),這類結構可以使脂解產物在腸道水溶性環境中保持穩定,且體積很小,極性較強。這些混合膠束將脂解產物傳遞至小腸上皮細胞的微絨毛表面,脂解后的產物通過被動擴散或蛋白質介導的方式進入小腸上皮細胞而被吸收。具體吸收機制根據脂質產物類型(如SCFA,MSCFA,LCPF和MAG)而有所不同。
2.1 短鏈和中鏈脂肪酸的吸收
短鏈脂肪酸(SCFA)和中鏈脂肪酸(MCFA)由于分子較小,水溶性較強,能夠通過被動擴散直接穿過小腸上皮細胞膜進入細胞。這些脂肪酸無需復雜的轉運過程,直接進入門靜脈系統并運送至肝臟進行代謝。此過程相對簡單,吸收效率較高。短、中鏈脂肪酸構成的甘油三脂經膽鹽乳化后在腸黏膜細胞內脂肪酶作用下水解成脂肪酸及甘油,通過門靜脈進入血循環。
2.2 長鏈脂肪酸的吸收
長鏈脂肪酸(LCFA)跨越細胞質膜的機制多年來一直存在爭議,核心問題在于這一過程是通過被動擴散發生還是由蛋白質介導的。早期研究認為,腸細胞對脂肪酸的攝取是通過被動擴散過程實現的,不依賴于蛋白質介導,只是濃度差異的自然擴散。然而,僅僅依賴于濃度梯度的被動擴散機制無法充分解釋一些現象,如脂肪酸攝取過程中的細胞特異性、高親和力以及對不同脂肪酸的選擇性。實際上,脂肪酸攝取的特異性與高親和力是依賴于轉運蛋白的協同作用。(1)CD36轉運蛋白:CD36是長鏈脂肪酸攝取的關鍵轉運蛋白之一,位于小腸近端腸上皮的刷狀邊緣處。CD36具有疏水性口袋結構,這使它能夠與LCFA結合,通過將脂肪酸導向細胞膜的外瓣葉(即細胞膜的外層),并在那里將其吸附到細胞膜表面。在CD36的作用下,結合的長鏈脂肪酸發生易位或翻轉,穿過細胞膜。一旦脂肪酸穿過細胞膜,它會與位于CD36胞內區域的脂肪酸結合蛋白(FABP)結合,FABP蛋白負責將LCFA轉運至細胞內部的不同代謝部位,比如線粒體、內質網、過氧化物酶體等,確保脂肪酸的高效再利用。(2)脂肪酸轉運蛋白4(FATP4):FATP4位于腸細胞膜上,可以直接與LCFA結合并將其轉運入細胞內。除了轉運脂肪酸外,FATP家族成員還具有酰基輔酶A合成酶的活性,能夠將進入細胞的LCFA快速轉化為脂酰輔酶A(acyl-CoA),從而鎖定脂肪酸在細胞內。FATP4是長鏈和超長鏈脂肪酸轉運的關鍵蛋白,可能的機制是通過FATP4將LCFA帶到細胞膜上,并降低LCPF跨膜的能量障礙,從而促進LCPF的擴散。(3)腸型脂肪酸結合蛋白(IFABP):一旦長鏈脂肪酸進入腸上皮細胞,它們與細胞內的IFABP結合,轉運至內質網等代謝部位,確保脂肪酸的高效再利用。
2.3 單甘脂的吸收
單甘脂(MAG)與長鏈脂肪酸類似,形成混合微膠束后運送至腸上皮細胞膜,可以通過簡單擴散和部分脂質轉運蛋白(如CD36和FATP4)輔助進入腸細胞。進入細胞后,MAG會在內質網中與LCFA再酯化生成甘油三酯(TAG),新合成的TAG一部分會轉移至細胞質參與細胞質脂滴的合成存儲能量,部分會形成乳糜顆粒,運輸至淋巴系統參與體循環。
2.4 膽固醇的吸收
膽固醇的吸收主要在小腸上皮細胞中進行,由膽固醇轉運蛋白 (NPC1L1) 介導的。NPC1L1分布在小腸刷狀緣膜上,能高效地結合膳食膽固醇和膽汁中回收的膽固醇分子,將其從小腸腔內轉運至腸細胞內,這一過程是膽固醇吸收的關鍵步驟。膽固醇進入腸細胞后,可以被內質網中的乙酰輔酶A膽固醇酰基轉移酶(ACAT)催化,生成膽固醇酯,使其更易于包裝到脂蛋白中。膽固醇酯主要會進入乳糜顆粒(CM),這些顆粒負責將膳食脂質從腸道運輸到淋巴系統,再進入血液循環。未酯化的膽固醇不會轉化為膽固醇酯,而是可以直接被整合到高密度脂蛋白(HDL)顆粒中,從而進入血液循環。
2.5磷脂的吸收
磷脂是膳食和膽汁中的重要成分,可以通過簡單擴散的方式直接穿過腸細胞膜進入細胞。研究表明,ATP結合盒轉運蛋白B4(ABCB4)可能在磷脂的跨膜運輸中發揮作用,但具體機制尚未完全明確。磷脂進入腸細胞后,磷脂可能與脂肪酸結合,形成新的磷脂分子,進一步進入內質網合成其他更復雜的脂類,如磷脂酰膽堿、磷脂酰乙醇胺等。吸收的磷脂部分會加入乳糜顆粒,通過淋巴系統運輸到血液;另一部分則可以直接形成高密度脂蛋白(HDL)顆粒并進入血液。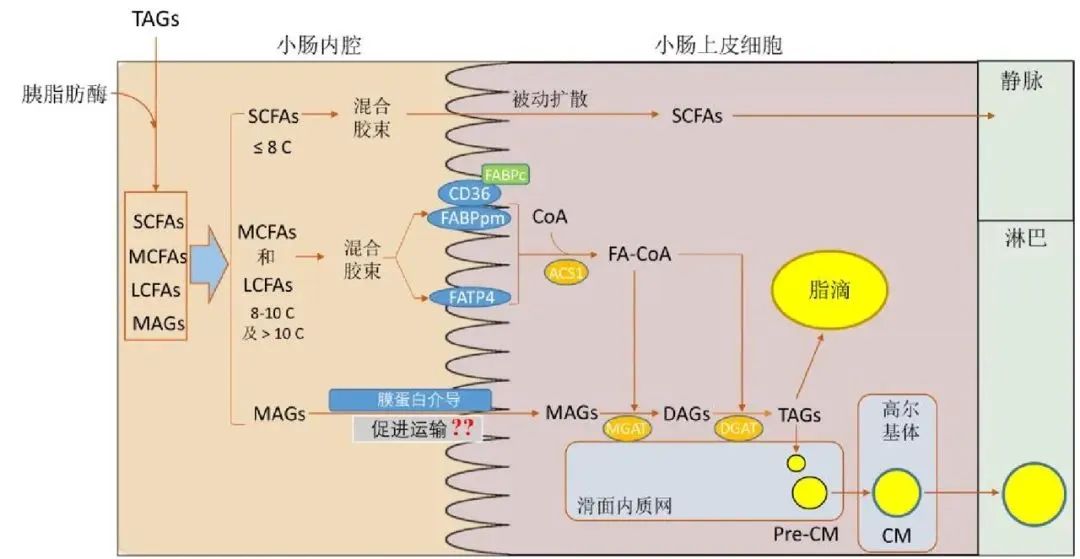
膳食油脂在腸道吸收過程中的分子機制
3. 脂肪酸的代謝與乳糜微粒的形成
膳食中的脂肪酸首先被乳化并形成微膠束,脂肪酸從這些微膠束中釋放出來,通過脂質膜進入腸上皮細胞內,進入腸上皮細胞的長鏈脂肪酸在內質網(endoplasmic reticulum, ER)中重新合成為甘油三酯。這一過程由一系列酶催化完成的,特別是甘油三酯合成酶在脂肪酸與甘油分子的重構中起關鍵作用。除甘油三酯外,吸收入細胞的游離膽固醇和磷脂也在腸細胞內進行重新合成,形成細胞所需的脂類。這些重新合成的脂質分子(如甘油三脂、膽固醇和磷脂)會與特定的蛋白質結合,形成乳糜微粒(chylomicrons)。乳糜微粒是一種包含甘油三酯、膽固醇、磷脂和脂溶性維生素的脂質運輸顆粒,外層由磷脂和蛋白質形成的單層膜包裹,能夠在水溶性血漿中穩定存在。乳糜微粒再通過胞吐作用(exocytosis)被釋放到腸上皮細胞的細胞間隙,隨后進入淋巴系統。
4. 乳糜微粒的轉運與脂肪酸的全身分布
乳糜微粒進入淋巴系統后,經過胸導管進入血液循環,逐漸被身體各個組織器官攝取和利用,特別是肝臟、肌肉和脂肪組織。在這些組織中,乳糜微粒中的脂質被代謝,提供細胞所需的能量,同時也是儲存脂質的重要形式。
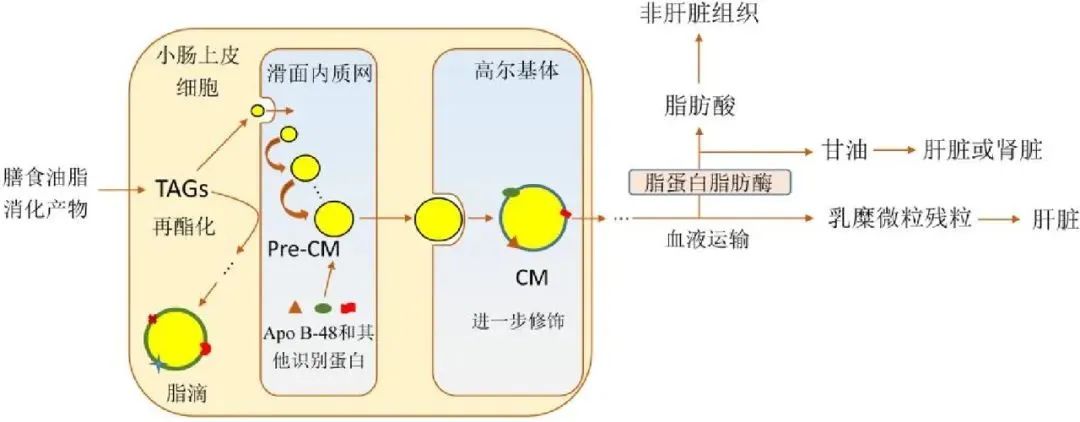
膳食油脂消化后的轉運及代謝過程
5. 油脂吸收的調控機制與影響因素
膳食油脂的吸收不僅依賴于消化系統的生理功能,還受到多種內外因素的調節。
5.1 膽汁酸的回收與脂肪酸吸收
膽汁酸在油脂吸收過程中發揮重要作用,其有效回收是保障脂肪酸高效吸收的關鍵。膽汁酸在回腸末端被重吸收,經過肝腸循環返回肝臟并重新分泌到膽囊,從而維持其在消化道中的穩定濃度。
5.2 激素的調控作用
胰島素、胰高血糖素樣肽-1(GLP-1)等胃腸激素在餐后分泌,作用于腸道上皮細胞和轉運蛋白,調節脂肪酸的吸收和代謝。此外,胰島素還調控脂肪酸的細胞內代謝,促進脂肪酸向脂肪組織儲存。
5.3 營養和膳食因素
膳食中的纖維、蛋白質、碳水化合物及其他微量營養素對脂肪酸的吸收有直接影響。例如,高膳食纖維可能通過增加腸內容物的黏度,減少脂肪酸與小腸上皮的接觸,從而降低脂肪酸的吸收率。此外,膳食中多不飽和脂肪酸的比例也會影響脂肪酸吸收的效率。
5.4 病理狀態對脂肪酸吸收的影響
某些疾病狀態可能影響脂肪酸的正常吸收,如胰腺功能不全、膽汁酸代謝障礙或小腸吸收不良綜合征。這些疾病通過干擾乳化、脂解或轉運過程,導致脂肪酸吸收障礙,進而影響全身的能量代謝。
6. 結論
脂肪酸的吸收是膳食油脂代謝中至關重要的環節,涉及多個復雜的生理過程和分子機制。油脂在腸道中經歷乳化、脂解、轉運和再合成等步驟,最終以乳糜微粒的形式進入淋巴系統,并通過血液循環輸送至全身各組織。脂肪酸的吸收過程受膽汁酸、轉運蛋白和激素等多重因素的調控,而其吸收效率則受到膳食組成、病理狀態等因素的影響。
參考文獻:
[1] Mansbach CM 2nd, Nevin P. Intracellular movement of triacylglycerols in the intestine[J]. J Lipid Res, 1998, 39(5):963-968.
[2] Mu H, H?y CE. The digestion of dietary triacylglycerols[J]. Prog Lipid Res, 2004, 43(2):105-133.
[3] Ko CW, Qu J, Black DD, et al. Regulation of intestinal lipid metabolism: current concepts and relevance to disease[J]. Nat Rev Gastroenterol Hepatol, 2020, 17(3):169-183.
[4] Xiao C, Stahel P, Lewis GF. Regulation of chylomicron secretion: Focus on post-assembly mechanisms[J]. Cell Mol Gastroenterol Hepatol, 2019, 7(3):487-501.
[5] 葉展. 典型膳食油脂胃腸道消化吸收特性及其對腸道健康的影響研究[D]. 江南大學, 2020.
注:文章內容來自脂質江南,文章轉載僅供大家學習、交流,如有版權問題請聯系作者刪除。